Probiotyki w insulinooporności stanowią dla mnie niesamowicie interesujący temat w kontekście wsparcia redukcji tego zaburzenia. Mikrobiota jelitowa bowiem i zmiany w obrębie jej składu ilościowego oraz jakościowego w ostatnich latach zostały powiązane z ich wpływem na rozwój m.in. otyłości, chorób sercowo-naczyniowych, depresji, PCOS, niealkoholowego stłuszczenie wątroby, zespołu jelita nadwrażliwego czy cukrzycy typu 2.
Wiele z wymienionych chorób wiąże się także ze współwystępującą z nimi insulinoopornością (IO), czyli stanem obniżonej wrażliwości tkanek docelowych na ten hormon, pomimo jego odpowiedniego lub wręcz zwiększonego stężenia we krwi. Czym jest dokładnie insulinooporność, przeczytasz w tym artykule.
Doskonale wiemy, że insulinooporność jest wstępem do wystąpienia cukrzycy typu 2, ale jednocześnie można się jej pozbyć i zminimalizować ryzyko pojawienia się choroby. Działaniami, które są niezbędne, by poprawić gospodarkę glukozowo-insulinową są:
- odpowiednia dietoterapia (o diecie w IO pisałam tutaj),
- regularna aktywność ruchowa,
- dbanie o sen,
- redukcja stresu,
- suplementacja, a wraz z nią także probiotykoterapia.
W świetle rosnącej liczby badań naukowych mikrobiota jelitowa może odgrywać znaczącą rolę w patogenezie cukrzycy typu 2, a także w stadium ją poprzedzającym, czyli właśnie u osób z insulinoopornością. Jak może wpływać na insulinooporność? W jaki sposób możesz sobie pomóc? Wszystkiego dowiesz się z tego artykułu.
PROBIOTYKI W INSULINOOPORNOŚCI – DYSBIOZA JELITOWA WINOWAJCĄ?
Insulinooporność jest stanem najczęściej diagnozowanym u osób z nadwagą i otyłością, spożywających tzw.. dietę zachodnią (wysokoprzetworzoną, z wysoką zawartością tłuszczów oraz cukrów prostych, ubogą w błonnik pochodzący m.in. z warzyw czy owoców, obfitującą w słodycze, słone przekąski, przetworzone dania gotowe) oraz u osób o bardzo niskiej aktywności ruchowej.
Często też przebiega wraz z problemami i chorobami endokrynologicznymi np. niedoczynnością tarczycy, endometriozą, zespołem policystycznych jajników (PCOS), chorobą Hashimoto. Tutaj mimo prawidłowej masy ciała, kobiety jak i mężczyźni mogą mieć współistniejącą insulinooporność. Warto jednak zaznaczyć, że szczupła sylwetka nie oznacza, że nie dochodzi do gromadzenia tkanki tłuszczowej w okolicach ważnych narządów w jamie brzusznej. Tzw. tkanka tłuszczowa wisceralna (brzuszna) może wpływać negatywnie na zdrowie u osób zarówno z prawidłową, jak i nadmierną masą ciała.
Niestety dieta zachodnia, nieodpowiednia masa ciała, a także popularność farmakoterapii czyli, częste przyjmowanie leków jak inhibitory pompy protonowej (stosowane np. w refluksie), szeroko dostępne środki przeciwbólowe, antybiotyki, do tego toksyny środowiskowe, przewlekły stres powodują, że mikrobiota jelitowa zmienia swój skład ilościowy i jakościowy co prowadzi do tzw. dysbiozy jelitowej.
Jeśli nie wiesz, czym jest dokładnie mikrobiota jelitowa, dysbioza jelitowa czy probiotyki, zapoznaj się z artykułem, który stanowi niejako słowniczek pojęć pomagający poruszać się w tym temacie z pełnym zrozumieniem.
Słowniczek pojęć o mikrobiocie – KLIK
Dysbioza jelitowa poprzez szereg różnych mechanizmów prowadzi do insulinooporności. W jaki sposób?
Omówię według mnie trzy najistotniejsze mechanizmy. Należą do nich:
- zwiększony pobór energii ze spożywanych pokarmów,
- zaburzenia szczelności bariery jelitowej skutkujące pogłębianiem się przewlekłego stanu zapalnego w organizmie,
- wpływ na spadek produkcji tzw. czynnika tkankowego indukowanego głodzeniem (z ang. FIAF), co w szeregu procesów prowadzi do lipotoksyczności (spokojnie, za chwilę to wyjaśnię prostszym językiem i wszystko stanie się jasne). 🙂
DYSBIOZA JELITOWA – OMÓWIENIE 3 PODSTAWOWYCH MECHANIZMÓW PROWADZĄCYCH DO ROZWOJU INSULINOOPORNOŚCI
1. MIKROBIOTA W INSULINOOPORNOŚCI – ZWIĘKSZONY POBÓR ENERGII ZE SPOŻYWANYCH POKARMÓW
Mikroorganizmy zasiedlające naszą mikrobiotę jelitową mają zdolność do wytwarzania hydrolaz glikozydowych, czyli enzymów, które są niezbędne w procesie rozkładania złożonych związków roślinnych, np. nierozpuszczalnego błonnika pokarmowego. Przez wiele lat myśleliśmy, że niestrawione resztki pokarmowe nie stanowią dla człowieka źródła dodatkowej energii, czyli mówiąc kolokwialnie, źródła kilokalorii. A to dlatego, że enzymy trawienne człowieka nie są w stanie ich strawić.
W sytuacji, w której są jednak rozkładane m.in. z powodu fermentacji prowadzonej przez bakterie, liczba kalorii, jaką pozyskuje w ten sposób nasz organizm dodatkowo, może wynosić od 4 do 10% energii czyli od 80 do 200 kcal dziennie. W perspektywie roku to dodatkowe od 29 200 kcal do 73 000 kcal, które można przeliczyć na 4 do 10,5 kg na wadze więcej!
To ogromna ilość energii, która przyczyniać się może – szczególnie u osób z nadwagą i otyłością – do pogłębiania trudności z redukcją masy ciała.
W innych badaniach wykazano, że mikrobiota jelitowa w wyniku hydrolizy i fermentacji krótkołańcuchowych kwasów tłuszczowych (masłowego, octowego i propionowego) w wyniku ich absorpcji, czyli wchłaniania, może zwiększać ilość przyswajanej energii (kilokalorii) o około 150 kcal dziennie.
Co więcej, kwas propionowy może być wykorzystywany przez ustrój do syntezy glukozy i lipidów, a także wpływać na zwiększony apetyt, spowolnienie pasażu jelitowego i spowolnienie motoryki jelit, co wiąże się ze zwiększonym czasem wchłanianie związków odżywczych i pozyskiwania z nich energii. To wszystko wpływa na zwiększenie bilansu energetycznego.
Mówiąc wprost, w wyniku dysbiozy jelitowej nasz organizm może sprawić, że dostarczamy więcej energii z pożywienia niż byśmy myśleli i chcieli. To może tłumaczyć fakt, dlaczego u niektórych osób mimo odpowiednich wyliczeń związanych z zapotrzebowaniem energetycznym i zastosowaniem delikatnie redukcyjnej diety, nie obserwuje się większych spadków masy ciała.
Innym mechanizmem tłumaczącym zwiększenie poboru energii z pożywienia jest zdolność niektórych rodzajów bakterii jelitowych do produkcji i wydzielania takich związków chemicznych, które powodują podwojenie gęstości naczyń włosowatych w nabłonku jelita cienkiego. To z kolei powoduje, że może dochodzić do zwiększonego wchłaniania w przewodzie pokarmowym cukrów prostych.
Nie jest to w żaden sposób zjawisko pożądane w przypadku osób z insulinoopornością, u których zbyt wysokie spożycie produktów je zawierających niekorzystnie wpływa na poziom glukozy na czczo oraz po posiłkach.
2. MIKROBIOTA W INSULINOOPORNOŚCI – ZABURZENIA SZCZELNOŚCI BARIERY JELITOWEJ SKUTKUJĄCE POGŁĘBIANIEM SIĘ PRZEWLEKŁEGO STANU ZAPALNEGO W ORGANIZMIE
Bariera jelitowa to struktura, która jest zbudowana z jednej warstwy komórek nabłonka jelitowego, która jest pokryta ochronną warstwą śluzu z bytującą w nim mikrobiotą. Pod nabłonkiem znajdują się komórki m.in. układu chłonnego, nerwowego, krwionośnego czy immunologicznego.
Ważnym elementem bariery jelitowej są między innymi tzw. połączenia ścisłe. Dzięki nim komórki ścisło do siebie przylegają i “decydują” co może, a co nie może przedostać się z przewodu pokarmowego do krwiobiegu. To dzięki połączeniom ścisłym antygeny czy metabolity bakteryjne nie przekraczają bariery jelitowej. Możesz to sobie wyobrazić jako bardzo ścisło ułożone obok siebie deski płotu. Gdy brak między deskami dużych szczelin, niewiele może się przez nie przedostać i o to przecież chodzi, prawda? Po to masz płot, by żadne intruzy nie dostały się na Twoje podwórko. Podobnie jest z połączeniami ścisłymi bariery jelitowej.
źródło grafiki: “Aptekarz Polski”, nr 158 (136e), październik 2019
Niestety bariera jelitowa traci swoją integralność, kiedy dochodzi do dysbiozy jelitowej. Może się to stać w wyniku:
- nasilonego, długotrwałego stresu,
- zakażenia bakteryjnego czy wirusowego/grzybiczego,
- z powodu stosowanej antybiotykoterapii czy farmakoterapii,
- nadmiernej konsumpcji alkoholu,
- nieodpowiedniej diety (także diety eliminacyjnej, przeprowadzanej na własną rękę w nierozsądny sposób),
- połączenia działania kilku czynników np. słabej jakości diety z długotrwałym stresem, deprywacją snu, niską aktywności ruchową i antybiotykoterapią.
W wyniku dysbiozy dochodzi do zmniejszenia produkcji ważnych białek, które wchodzą w skład połączeń ścisłych, czyli zonuliny i okludyny, oraz innych ważnych elementów związanych z integralnością bariery jelitowej. To powoduje, że połączenia “rozluźniają się”. Wykorzystując przykład z płotem, powstają większe szczeliny między deskami, a wiele substancji szkodliwych przenika do krwiobiegu powodując, tzw. endotoksemię.
Co przenika przez nieszczelną barierę jelitową? Antygeny, patogeny, fragmenty ścian bakterii gram-ujemnych nazywane lipopolisacharydami (LPS).
Niestety endotoksemia sprzyja wzrostowi tkanki tłuszczowej w organizmie, nasila stan zapalny oraz przyczynia się do kolejnych problemów zdrowotnych, czyli zaburzeń metabolicznych, insulinooporności i zwiększonego ryzyka wystąpienia cukrzycy typu 2, chorób sercowo-naczyniowych czy problemów natury hormonalnej.
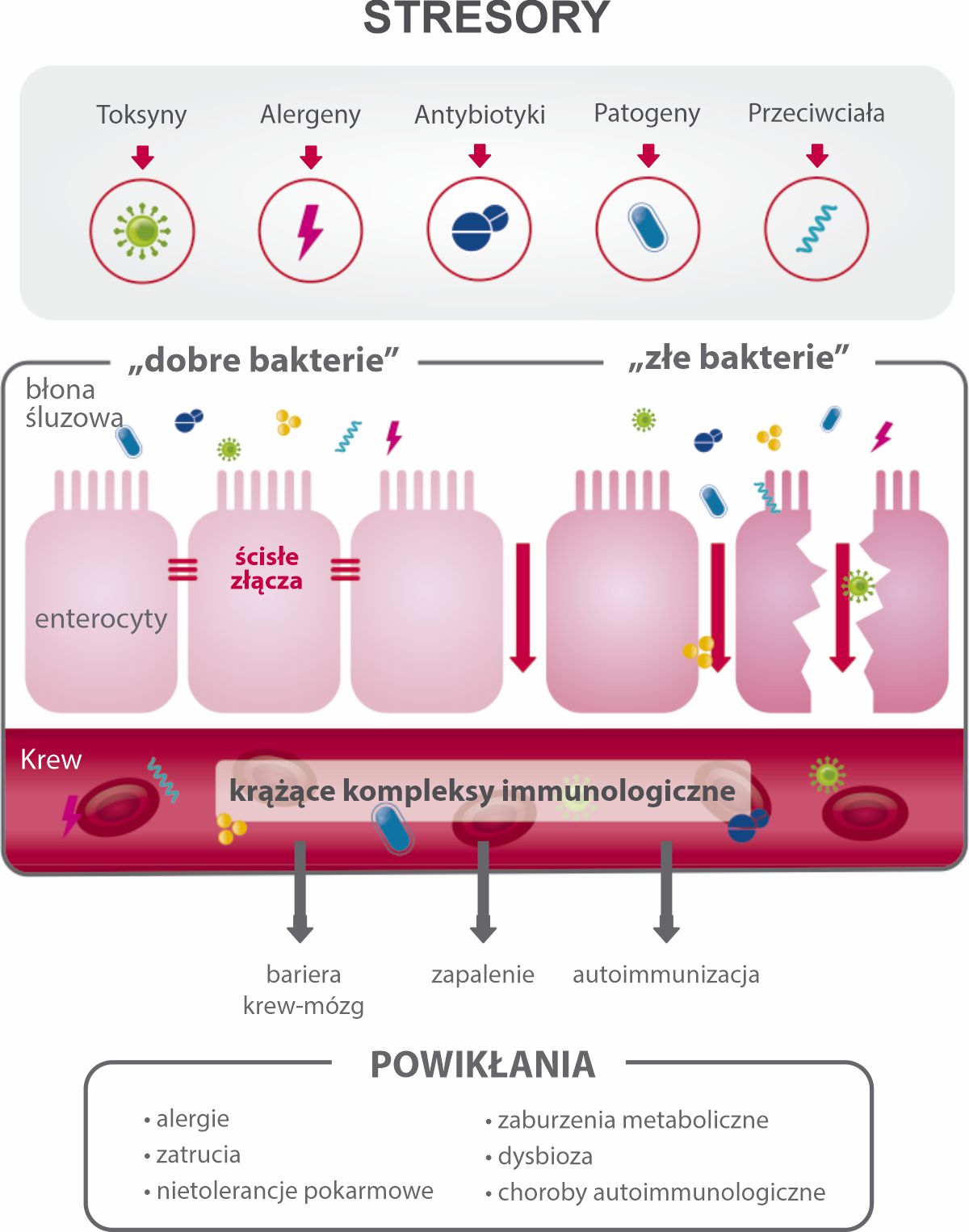
Na poniższej, uproszczonej grafice widzisz, co powoduje uszkodzenia bariery jelitowej. Gdy połączenia ścisłe (lewa strona grafiki z napisem “dobre bakterie”) są zachowane, żadne toksyny, alergeny czy patogeny nie przedostają się do krwi. Po prawej stronie (z napisem “złe bakterie) w przypadku rozluźnienia się połączeń ścisłych toksyny, patogeny czy przeciwciała przenikają do krwi, powodując m.in. stan zapalny. Powikłań takiego stanu jest naprawdę dużo i mają one ogromny wpływ na nasze zdrowie.
źródło grafiki: Aptekarz Polski”, nr 158 (136e), październik 2019
3. WPŁYW NA SPADEK PRODUKCJI CZYNNIKA TKANKOWEGO INDUKOWANEGO GŁODZENIEM
Ostatnim mechanizmem, który łączy zaburzenia mikrobioty jelitowej z insulinoopornością to spadek produkcji czynnika tkankowego indukowanego głodzeniem (fasting-induced adipocyte factor – FIAF).
Czynnik ten powoduje, że dochodzi do hamowania działania lipazy lipoproteinowej. To niekorzystny efekt, ponieważ zwiększa uwalnianie kwasów tłuszczów i ich odkładanie w komórkach tłuszczowych m.in. wątroby. Gdy dochodzi do sytuacji, w której możliwości magazynowania kwasów tłuszczowych w komórce tłuszczowej się wyczerpują, czyli mamy do czynienia z przeładowaniem, pojawia się zjawisko lipotoksyczności.
Możesz sobie wyobrazić, że komórka tłuszczowa, czyli adipocyt jest jak otwierana kuleczka. Do takiej kuleczki możesz wlać określoną ilość wody czy włożyć określoną ilość piasku. Dokładnie tak samo jest z adipocytem. Jest w stanie pomieścić tylko określoną ilość tłuszczu.
Niestety upakowane po brzegi komórki tłuszczowe zaczynają produkować duże ilości cytokin prozapalnych i jak sama nazwa wskazuje, nasilają one dodatkowo stan zapalny, co więcej, powodują też zaburzenia sygnalizacji insuliny, co ma miejsce oczywiście w insulinooporności.
Wydzielanie insuliny może być też zaburzone przez negatywny wpływ zaburzonej mikrobioty na działanie innych związków np. inkretyn (glukozozależny peptyd insulinowy – GIP czy glukagonopodobny peptyd 1 – GLP-1).
Jak widzisz, wszystkie omówione mechanizmy wpływają na powstawanie insulinooporności, a każdy z nich jest związany z dysbiozą jelitową, czyli, dla przypomnienia, zaburzeniem ilościowym i jakościowym mikroorganizmów budujących naszą mikrobiotę jelitową.
No dobrze. Wiesz już, jak dysbioza jelitowa wpływa na powstawanie insulinooporności i pogłębianie się tego zaburzenia metabolicznego. Co zatem można zrobić, by ogarnąć ten metaboliczny bałagan?
MIKROBIOTA JELITOWA W INSULINOOPORNOŚCI – CO ZROBIĆ, BY POZBYĆ SIĘ DYSBIOZY?
Jako dietetyczka nie mogę zacząć od innej drogi niż zmiana stylu życia. Powtarzam to w kółko: dieta, ruch, sen, regeneracja i odpoczynek, redukcja stresu i suplementacja dobrana indywidualnie to podstawa. Przyjrzenie się przyjmowanym lekom (może nadużywasz środków przeciwbólowych, może ciągle zażywasz leki na zgagę, pijesz sporo alkoholu, palisz papierosy?).
W suplementacji bardzo ważne jest zastosowanie odpowiedniego probiotyku, o udowodnionym działaniu naukowym, który ma wpływ na wskazane przeze mnie mechanizmy powstawania insulinooporności.
Trudno też nie wspomnieć o tym, że metformina przepisywana pacjentom z insulinoopornością, często niestety nadużywana, nie pozostaje bez wpływu na mikrobiotę. Wiele badań wskazuje na to, że zaburza ona funkcjonowanie mikrobioty jelitowej. Dlatego ważne jest, by możliwie jak najwięcej wysiłku i działania kierować w zmianę stylu życia. U większości moich Podopiecznych pozwalało to albo uniknąć farmakoterapii, albo znacząco zmniejszyć liczbę stosowanych leków i w istocie pozbyć się insulinooporności za pomocą diety, ruchu i celowanej suplementacji.
PROBIOTYKI W INSULINOOPORNOŚCI
Jako że tematem artykułu jest mikrobiota jelitowa i jej modulacja, czas na omówienie probiotyków, które mogą wesprzeć osoby z insulinoopornością w jej redukcji i poprawie stanu zdrowia. Chcę bowiem podkreślić, że to właśnie skuteczne uszczelnianie bariery jelitowej, przywrócenie równowagi mikrobioty i zmniejszanie stanu zapalnego będą kluczowymi elementami redukcji insulinooporności na poziomie metabolicznym. I tego też oczekuje się od dobrego probiotyku.
Przeprowadzono szereg badań naukowych, które oceniały wpływ probiotykoterapii na zaburzenia metaboliczne, w tym insulinooporność, ale też na parametry metaboliczne związane z dysbiozą jelitową u osób z cukrzycą typu 2. Badano wpływ probiotyków na wskaźnik HOMA-IR, parametry stanu zapalnego w organizmie, zwiększaniu szczelności bariery jelitowej, zmniejszenie liczby cytokin prozapalnych czy endotoksemii.
Przyjmowanie probiotyków wiąże się z modulacją, czyli zmianami w obrębie mikrobioty jelitowej m.in. poprzez zwiększenie liczby pałeczek kwasu mlekowego czy bakterii z rodzaju Bifidobacterium. To bardzo korzystne działanie, które prowadzi do poprawy szczelności bariery jelitowej, ograniczenia stanu zapalnego, endotoksemii, a więc i w konsekwencji do poprawy insulinowrażliwości (komórki stają się bardziej wrażliwe na działanie insuliny), co w dalszej kolejności przyczynia się do poprawy funkcjonowania gospodarki glukozowo-insulinowej.
Ważne jest jednak podkreślenie, że nie każdy probiotyk będzie wykazywał właściwości sprzyjające redukcji insulinooporności. Działanie probiotyków jest specyficzne, a konkretny probiotyk musi mieć udokumentowane działanie kliniczne. Probiotyki odpowiednie do stosowania przy biegunce czy po antybiotykoterapii to nie te same probiotyki, które są stosowane np. w kolce niemowlęcej czy redukcji insulinooporności.
PROBIOTYKI W INSULINOOPORNOŚCI – CO MÓWIĄ BADANIA?
W 2018 r zespół badaczy pod kierownictwem M. Szulińskiej, grupie 81 kobiet w wieku około- i pomenopauzalnym podawał probiotyk Sanprobi Barrier zawierający 9 szczepów probiotycznych. Kobiety dotyczył problem otyłości. Z powodu obniżonej produkcji estrogenów w grupie takich kobiet występuje szczególne ryzyko problemów metabolicznych, w tym insulinooporności, ale też kardiologicznych.
Po 12 tygodniach przyjmowania probiotyku odnotowano:
- istotny spadek poziomu lipopolisacharydu (wpływa na endotoksemię i stan zapalny),
- zmniejszenie obwodu pasa i ilości tkanki tłuszczowej,
- zmniejszenie zawartości cholesterolu całkowitego i LDL (tzw. złego cholesterolu) we krwi,
- zmniejszenie stężenia glukozy, insuliny oraz wskaźnika HOMA-IR,
- redukcję kwasu moczowego w surowicy krwi.
W innym badaniu sprawdzającym wpływ probiotykoterapii na zmniejszenie sztywności tętnic i poprawę funkcji naczyń krwionośnych, po 12-tygodniowym podaniu probiotyku Sanprobi Barrier, odnotowano m.in.:
- zmniejszenie stężenia cytokin prozapalnych,
- skurczowego ciśnienia tętniczego,
- redukcję markerów dysfunkcji śródbłonka jelitowego. Pamiętasz jeszcze, że ma to wpływ na zaburzenia integralności bariery jelitowej i na insulinooporność?
W obu badaniach zaobserwowano, że liczba przyjmowanych bakterii ma znaczenie. Korzystniejsze wyniki uzyskano w grupach z większą dawką czyli 1x 1010 CFU (jednostek tworzących kolonię).
W 2017 r. Sabico i wsp., na grupie osób z cukrzycą typu 2 nieleczonych farmakologicznie, po zastosowaniu probiotykoterapii również odnotowali obniżenie wskaźnika HOMA-IR, a także redukcję insuliny i glukozy na czczo, lipopolisacharydu (LPS), cytokin prozapalnych. Co ciekawe, po 12 tygodniach zmniejszyło się również stłuszczenie okolic brzucha, co ma korzystny wpływ na zwiększenie insulinowrażliwości.
W opublikowanym w 2016 roku przeglądzie badań dotyczących stosowania probiotyków w otyłości, insulinooporności, cukrzycy typu 2 i niealkoholowym stłuszczeniu wątroby przez M.L. Saez-Lara i wsp. na 17 interwencji probiotykoterapeutycznych, które trwały od 4 do 36 tygodni, tylko w 3 trzech nie zanotowano efektów. Przegląd badań klinicznych brał też pod uwagę zastosowanie synbiotyków, czyli połączenia probiotyku z prebiotykiem.
Zdaje się jednak, że najważniejszym udokumentowaniem działania probiotyków w kontekście redukcji insulinooporności jest metaanaliza opublikowana na podstawie 61 badań z randomizacją (to takie wysokiej jakości badania kliniczne) w 2020 roku.
Wnioski z metaanalizy wskazywały na korzystny wpływ probiotykoterapii na czynniki indukujące insulinooporność, np. wskaźnik BMI, obwód talii, redukcję stanu zapalnego czy zmniejszenie stężenie cholesterolu całkowitego we krwi.
Jako taki mały smaczek (bo temat będę omawiała szerzej), w 2018 roku opublikowano metaanalizę badań związaną z zastosowaniem probiotykoterapii i jej wpływem na poziom glukozy we krwi u kobiet w ciąży.
Wniosek jaki przytoczyli badacze, brzmi: probiotyki zmniejszają stężenie glukozy u kobiet w ciąży, szczególnie bez rozpoznanej cukrzycy typu 2. Dalsze badania są oczywiście wskazane, ale chciałam dodać, że kobiety w ciąży i ich zmieniająca się gospodarka hormonalna oraz glukozowo-insulinowa, która prowadzi do fizjologicznej insulinooporności jest niestety połączona z wysokim ryzykiem rozwoju cukrzycy ciążowej. Odpowiednia kontrola glikemii ma tu znaczenie i probiotyki są w tym bardzo pomocne.
PROBIOTYKI W INSULINOOPORNOŚCI – PODSUMOWANIE
Insulinooporność to stan metaboliczny, który można cofnąć, a zmiany, które wprowadzają moi Podopieczni są związane przede wszystkim z tym, by zastosować odpowiednią dietę i wdrożyć codzienny ruch do swojego życia.
Wsparciem w redukcji insulinooporności są także ważne elementy naszego życia, jak dobry, jakościowy sen, odpoczynek, czas dla siebie i zastosowanie odpowiednio wspierającej, intensyfikującej działania suplementacji. Probiotyki, takie jak Sanprobi Barrier, które wspierają odzyskanie równowagi w obrębie mikrobioty jelitowej są kluczowe w redukcji insulinooporności na poziomie metabolicznym. Wspierają prawidłową gospodarkę glukozowo-insulinową poprzez zmniejszanie dysbiozy jelitowej, a tym samym m.in. stanu zapalnego, lipotoksyczności i endotoksemii. Może to wydawać się skomplikowane dla przeciętnej osoby borykającej się z insulinoopornością, ale przekłada się na tak zrozumiałe parametry, jak: obniżenie stężenia glukozy i insuliny w wynikach badań, poprawę stężenia cholesterolu, lepsze samopoczucie czy ubytek masy ciała. To namacalne zmiany, o które warto powalczyć. Podsumowując, probiotyki w insulinooporności są nieocenionym wsparciem i odpowiednio zastosowane mają duży potencjał terapeutyczny.
Artykuł powstał we współpracy z partnerem merytorycznym – marką Sanprobi.
BIBLIOGRAFIA
- Gałęcka M. i wsp. Znaczenie mikrobioty jelitowej w kształtowaniu zdrowia człowieka — implikacje w praktyce lekarza rodzinnego, Forum Medycyny Rodzinnej ISSN 1897–3590
- Majewska K. i wsp. Mikroflora przewodu pokarmowego i jej rola w patogenezie cukrzycy typu 2, Farmacja Współczesna 2017; 10: 158-162
- Pokrzywnicka P., Gumprecht J., Mikrobiota i jej związek z cukrzycą typu 2 i otyłością, Diabetologia Praktyczna 2016, tom 2, nr 5
- M. Szulińska i wps.., Dose-Dependent Effects of Multispecies Probiotic Supplementation on the Lipopolysaccharide (LPS) Level and Cardiometabolic Profile in Obese Postmenopausal Women: A 12-Week Randomized Clinical Trial, „Nutrients” 2018, 10
- Sabico S. i wsp. Effects of a 6-month multi-strain probiotics supplementation in endotoxemic, inflammatory and cardiometabolic status of T2DM patients: A randomized, double-blind, placebo-controlled trial. Clin Nutr. 2019 Aug;38(4):1561-1569
- Ostrowska L. Wpływ mikrobioty jelitowej na zaburzenia metaboliczne i otyłość — punkt widzenia internisty i dietetyka, Gastroenterologia Kliniczna 2016, tom 8, nr 2, 62–73
- Basińska Anna M. Rola mikrobioty jelitowej i wsparcia probiotycznego w dietoteraii nadwagi i otyłości, dostęp z dnia 3.03.2022 https://www.wspolczesnadietetyka.pl/leczenie-nadwagi-i-otylosci/rola-mikrobioty-jelitowej-i-wsparcia-probiotycznego-w-dietoterapii-nadwagi-i-otylosci
- Skonieczna-Żydecka K. i wsp. “The Effect of Probiotics and Synbiotics on Risk Factors Associated with Cardiometabolic Diseases in Healthy People—A Systematic Review and Meta-Analysis with Meta-Regression of Randomized Controlled Trials”, J Clin Med. 2020 Jun; 9(6): 1788.
- 9.Tzu-Rong Peng i wsp. Effect of Probiotics on the Glucose Levels of Pregnant Women: A Meta-Analysis of Randomized Controlled Trials, Medicina (Kaunas). 2018 Nov; 54(5): 77