Akkermansia muciniphila (w skrócie AM), czyli wyjątkowa i korzystna dla naszego zdrowia bakteria, została odkryta niecałe dwie dekady temu. Mimo tej, zdaje się niedługiej kariery naukowej, zrewolucjonizowała podejście do probiotykoterapii, a także sposób patrzenia na gram-ujemne bakterie w środowisku badaczy.
Co więcej, korzystne efekty stosowania bakterii Akkermansia muciniphila MucT zostały w tym czasie przełożone na wiele interwencji klinicznych z udziałem zwierząt, a także ludzi, które potwierdzają jej wspierające działanie w kontekście zespołu metabolicznego, otyłości, cukrzycy, chorób sercowo-naczyniowych, czy chorób zapalnych jelit.
Na dobry początek polecam Ci przeczytać więcej o samej bakterii i jej wwyjątkowych właściwościach w artykule: Akkermansia muciniphila – bakteria do zadań specjalnych.
AKKERMANSIA MUCINIPHILA – BADANIA Z UDZIAŁEM ZWIERZĄT
Punktem wyjścia do badań klinicznych, sprawdzających działanie AM, była jej liczebność w przebadanych próbkach kału ludzi i zwierząt. Okazywało się, że liczebność bakterii jest znacznie zmniejszona u osób z nadwagą i chorobą otyłościową, cukrzycą typu 2, w chorobach zapalnych jelit (wrzodziejącym zapaleniu jelita grubego, chorobie Leśniowskiego-Crohna), a także w chorobach sercowo-naczyniowych i w niealkoholowej stłuszczeniowej chorobie wątroby. Niektóre badania wykazały także związek liczebności bakterii ze zmniejszonym stężeniem leptyny – hormonu odpowiedzialnego za odczuwanie sytości po posiłku.
Szereg badań w ostatniej dekadzie wykazało, że osoby z nadwagą i chorobą otyłościową, w porównaniu z osobami szczupłymi, mają niższe stężenie leptyny w organizmie. Co więcej, dochodzi u nich do leptynooporności, czyli zmniejszonej wrażliwości tkanek na działanie leptyny. Mówiąc prosto, leptynooporność sprawia, że jedzenie nie syci tak efektywnie, a odczuwany głód prowokuje zjadanie kolejnych posiłków, prowadząc do nadwyżki kalorycznej i tycia.
W poprzednich artykułach wspominałam, że mikrobiota jelitowa społeczeństw uprzemysłowionych różni się od tej, którą reprezentują społeczności i plemiona żyjące w sposób najbardziej zbliżony do zbieracko-łowieckiego, a więc z dala od cywilizacji zachodniej.
Analiza porównawcza mikrobiomu jelitowego uprzemysłowionych populacji zachodnich z mikrobiomem jelitowym plemienia Hadza również wykazała zmniejszenie liczebności bakterii z rodzaju Bacteroidia i Verrucomicbiota (należy od niego właśnie Akkermansia muciniphila).
W oparciu o wyniki badań na gryzoniach dokonano obserwacji, że suplementacja Akkermansią muciniphila wspierała poprawę szeregu parametrów metabolicznych.
U myszy karmionych dietą wysokotłuszczową podanie AM skutkowało:
- zmniejszeniem masy ciała,
- redukcją stężenia glukozy we krwi na czczo,
- poprawą insulinoowrażliwości (tkanki organizmu lepiej reagowały na insulinę, a więc dochodziło do zmniejszenia insulinooporności),
- zmniejszeniem stłuszczenia wątroby.
 źródło: Anhê and Marette Nature Medicine 2017
źródło: Anhê and Marette Nature Medicine 2017
Dodatkowo zmniejszał się stan zapalny oraz steżenie lipopolisacharydu (LPS), który jest endotoksyną i wykazuje szereg niekorzystnych zmian na poziomie ustrojowym.
W modelu mysim potwierdzono również, że suplementacja pasteryzowaną Akkermansią muciniphilą korzystnie wpływa także na obniżenie stężenia cholesterolu i trójglicerydów. Zmniejszenie dyslipidemi, czyli zaburzeń lipidowych, jest ważne dla zdrowia kardiologicznego.
Udowodniono także, że suplementacja AM u myszy wpływała na metabolizm lipidów w wątrobie i zapobiegała stłuszczeniu tego organu. Dochodziło do polepszenia tolerancji glukozy i zmniejszenia przyrostu tkanki tłuszczowej u otyłych myszy spowodowanego nieodpowiednią dietą.
W innych badaniach zaobserwowano, że stosowanie Akkermansii korzystnie wpływało na obniżenie stężenia enzymów wątrobowych i redukcję ogólnoustrojowego stanu zapalnego wywoływanego przez żywienie typu zachodniego, czyli m.in. wysokotłuszczowego.
Warto dodać, że w badaniach korzystny efekt suplementacji Akkermansią został udowniodniony zarówno dla formy żywej (probiotyk), jak i formy pasteryzowanej (postbiotyk). Co ciekawe, myszy otrzymujące formę pasteryzowaną wykazały większą redukcję masy ciała i tkanki tłuszczowej, zaobserwowano również większy spadek glukozy i insuliny na czczo.
To bardzo ważna obserwacja, ponieważ pasteryzowana Akkermansia muciniphila jest znacznie bardziej stabilna, ma znacznie dłuższy okres przydatności do spożycia, a w związku z tym jej dystrybucja staje się łatwiejsza. Stabilność pasteryzowanej AM wpływa korzystnie tym samym na czas i sposób przechowywania.
AKKERMANSIA MUCINIPHILA – BADANIA Z UDZIAŁEM LUDZI
Po bardzo korzystnych wynikach badań na zwierzętach przystąpiono do sprawdzenia, jak bakteria będzie wpływała na ludzi. I czy jest dla nich bezpieczna.
W pierwszym podwójnie zaślepionym badaniu Dopommier i wsp., którego celem było sprawdzenie hipotezy o korzystnym działaniu AM na ludzi, tzw. proof-of-concept, dorosłe osoby ze zdiagnozowanym stanem przedcukrzycowym i zespołem metabolicznym podzielono na trzy grupy:
- grupę kontrolną (placebo),
- grupę otrzymującą 1010 komórek Akkermansii muciniphila MucT w postaci żywej,
- grupę otrzymującą 1010 komórek Akkermansii muciniphila MucT w postaci pasteryzowanej (nieżyjącej bakterii).
Osoby zakwalifikowane do badania, co bardzo ważne dla jego wyników, nie zmieniały diety ani aktywności ruchowej w jego trakcie.
Badanie udowodniło, że Akkermansia muciniphila jest skuteczna i bezpieczna dla ludzi.
Bezpieczeństwo sprawdzano na wielu etapach 3-miesięcznego badania. Na żadnym z nich nie odnotowano zmian w stężeniu markerów związanych z zapaleniem wątroby, nerek czy mięśni.
Badanie to potwierdziło, że Akkermansia przynosi korzyści metaboliczne bez interwencji w zakresie diety i aktywności ruchowej. Jakie dokładnie?
Zaobserwowano:
- zmniejszenie masy ciała o około 2,27 kg, masy tłuszczu i około 1,37 kg i obwodu bioder o około 2,63 cm w grupie uczestników przyjmujących pasteryzowaną Akkermansię w porównaniu z placebo,
- zmniejszenie obwodu talli o około 1,56 cm, ale wartość ta nie osiągnęła istotności statystycznej,
- obniżenie stężenia insuliny o około 30% u obu grup przyjmujących Akkermansię (niezależnie od formy) w stosunku do grupy kontrolnej (placebo),
- poprawienie wskaźnika wrażliwości na insulinę o 30% w grupie przyjmującej pasteryzowaną AM w porównaniu z grupą placebo,
- zmniejszenie stężenia cholesterolu całkowitego o 8,68%, cholesterolu frakcji LDL o 7,53% i trójglicerydów o 15,71%, w grupie przyjmującej pasteryzowaną AM w porównaniu z grupą placebo,
- obniżenie liczby białych krwinek (WBC) w obu grupach przyjmujących AM w porównaniu z grupą kontrolną (podwyższone wartości WBC obserwuje się w chorobie otyłościowej, nietolerancji glukozy i osób z cukrzycą typu 2, przez co uznaje się podwyższenie tego wskaźnika jako predyktor wystąpienia cukrzycy typu 2),
- znaczące obniżenie endotoksyny LPS (lipopolisacharydu) w grupie przyjmującej pasteryzowaną AM,
- zmniejszenie stężenia dehydrogenazy mleczanowej (LDH) oraz kinazy kreatynowej (CK) w grupie stosującej pasteryzowaną AM (LDH i CK są wskaźnikami uszkodzenia tkanek i urazów specyficznych dla mięśni).
Dodatkowo badacze zmierzyli liczebność Akkermansii przed badaniem oraz po badaniu w kale uczestników. W obu grupach przyjmujących Akkermansię w postaci żywej i pasteryzowanej zwiększyła się liczebność bakterii. Nie miało to jednak wpływu na statystycznie istotne zmiany w składzie mikrobioty.
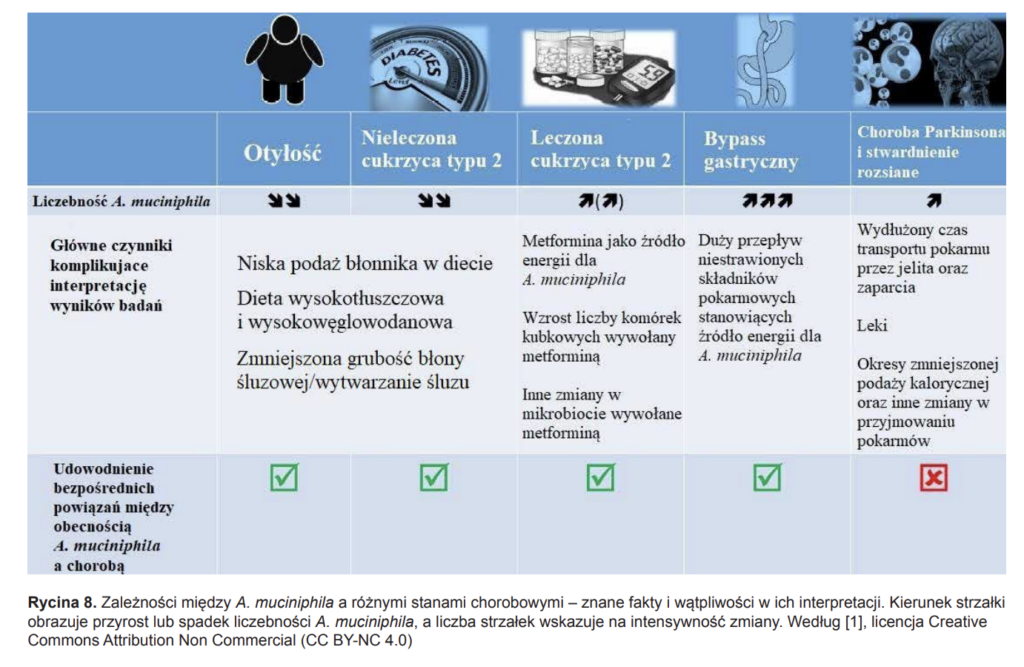
Źródło: Markowska E, Kiersztan A. Akkermansia muciniphila – obiecujący kandydat na probiotyk nowej generacji, Postępy Higieny i Medycyny Doświadczalnej, Vol. 75/2021 • 724-748
W innym badaniu klinicznym, w którym zastosowano mieszaninę probiotyczną wraz z Akkermansią muciniphilą i dodatkiem inuliny u pacjentów z cukrzycą typu 2, zaobserwowano poprawę poposiłkowego stężenia insuliny i glukozy. W badaniu dostrzeżono także korzystne skutki metaboliczne ograniczenia spożycia kalorii przez badanych, co autorzy powiązali z Akkermansią muciniphilą.
W innych badaniach u pacjentów z cukrzycą, którzy stosowali metforminę, odkryto wyższe stężenie AM. Rzuca to nowe światło na mechanizm działania leku, który może być tak skuteczny m.in. za sprawą Akkermansii.
Wyniki badań na zwierzętach i ludziach oraz wnioski z badania Mikrobes4U doprowadziły do uznania pasteryzowanej formy Akkermansii muciniphila MucT jako nowej żywności (novel food) przez EFSA. Suplementacja jest więc bezpieczna i potwierdzona u osób powyżej 18 roku życia.
Warto dodać, że badacze, formułując wnioski z dotychczasowych badań są właściwie zgodni: na ten moment stosowanie Akkermansi może istotnie wspierać terapię zaburzeń metabolicznych, jednocześnie nie zastąpi leczenia konwencjonalnego.
Interwencje z zakresu zmiany stylu życia oraz wdrażane leczenie farmakologiczne w konkretnych jednostkach chorobowych stanowi najważniejszy element terapii.
Zmiana stylu życia obejmuje interwencje w zakresie diety, aktywności ruchowej, snu, zrezygnowania z używek oraz odpowiedniego wypoczynku. Dieta, która według badań naukowych od ponad 20 lat uznawana jest za najzdrowszą, a przy okazji wpływającą niezwykle korzystnie na mikrobiotę jelitową, to dieta śródziemnomorska. Przeczytaj artykuł: dieta odżywiająca mikrobiotę jelitową.
W kolejnym artykule dowiesz się co dokładnie możesz zrobić, by zwiększyć liczebność Akkermansii za pomocą konkretnych strategii dietetycznych. Innym sposobem jest zastosowanie suplementacji postbiotykiem Sanprobi Premium The Akkermansia Company. To aktualnie jedyny na świecie preparat zawierający czystą postać pasteryzowanej bakterii.
PODSUMOWANIE
Akkermansia muciniphila MucT w formie pasteryzowanej to skuteczny element wsparcia leczenia zaburzeń metabolicznych, które przebiegając z uogólnionym stanem zapalnym, mają wpływ na zwiększone ryzyko wielu chorób. Odpowiednia liczebność bakterii w naszym jelicie korzystnie wpływa na regulację stężenia glukozy, cholesterolu, trójglicerydów i insuliny. Wspiera prawidłowe funkcjonowanie wątroby, zapobiegając jej stłuszczeniu. Suplementacja tym szczepem wykazuje także wsparcie w redukcji masy ciała bez zmiany w zakresie diety i aktywności ruchowej, co oczywiście nie oznacza, że sama suplementacja zrobi wszystko za nas. 🙂
Artykuł powstał we współpracy z marką Sanprobi.
BIBLIOGRAFIA
- Cani PD i wsp. Akkermansia muciniphila: paradigm for next-generation beneficial microorganisms. Nat Rev Gastroenterol Hepatol. 2022 Oct;19(10):625-637. doi: 10.1038/s41575-022-00631-9. Epub 2022 May 31. Erratum in: Nat Rev Gastroenterol Hepatol. 2022 Jun 23;: PMID: 35641786.
- Depommier C i wsp. Supplementation with Akkermansia muciniphila in overweight and obese human volunteers: a proof-of-concept exploratory study. Nat Med. 2019 Jul;25(7)
- Zhang H, et al. White blood cell subtypes and risk of type 2 diabetes. J Diabetes Complications. 2017;31:31–37
- Druart C, Plovier H, Van Hul M, Brient A, Phipps KR, de Vos WM, Cani PD. Toxicological safety evaluation of pasteurized Akkermansia muciniphila. J Appl Toxicol. 2021 Feb;41(2)
- Li J, et al. Gut microbiota dysbiosis contributes to the development of hypertension. Microbiome. 2017;5:14.
- Markowska E, Kiersztan A. Akkermansia muciniphila – obiecujący kandydat na probiotyk nowej generacji, Postępy Higieny i Medycyny Doświadczalnej, Vol. 75/2021 • 724-748
- https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6924600/
- https://academic.oup.com/edrv/article/40/5/1271/5487987?login=false
- https://www.nature.com/articles/nm.4261.epdf
- https://www.ingutwetrust.org/akkermansia-muciniphila-making-of/
- https://www.frontiersin.org/articles/10.3389/fgstr.2022.1024393/full






